
Rev. Ciencias Veterinarias, Vol. 44, N° 1, [1-11], E-ISSN: 2215-4507, enero-junio, 2026
DOI: https://doi.org/10.15359/rcv.44-1.1
URL: http://www.revistas.una.ac.cr/index.php/veterinaria/index
Caracterización molecular de Taenia saginata en bovinos sacrificados en mataderos de Costa Rica
Molecular characterization of Taenia saginata in cattle slaughtered in Costa Rica
Caracterização molecular de Taenia saginata em bovinos abatidos em matadouros da Costa Rica
Elisa Alcántara-Henríquez1.2  , Gaby Dolz, 1.3
, Gaby Dolz, 1.3
1 Universidad Nacional, Posgrado Regional en Ciencias Veterinarias (PCVET), Maestría en Enfermedades Tropicales, Campus Benjamín Nuñez, Barreal de Heredia, P.O. Box 86. 3000 Heredia, Costa Rica. elisa.alcantara@unah.edu.hn,
 https://orcid.org/0009-0005-5076-3107
https://orcid.org/0009-0005-5076-3107
2 Present address: Universidad Nacional Autónoma de Honduras, E Facultad de Ciencias, Escuela de Microbiología, Departamento de Parasitología, , Código Postal 11101, Tegucigalpa, Honduras.
3 Universidad Nacional, Escuela de Medicina Veterinaria, Programa de Investigación en Medicina Poblacional, Laboratorio de Zoonosis y Entomología, Campus Benjamín Nuñez, Barreal de Heredia, P.O. Box 86, 3000 Heredia, Costa Rica. gaby.dolz.wiedner@una.ac.cr,  https://orcid.org/0000-0002-9566-5130
https://orcid.org/0000-0002-9566-5130
 Autor de correspondencia: elisa.alcantara@unah.edu.hn
Autor de correspondencia: elisa.alcantara@unah.edu.hn
Recibido: 4 diciembre 2024 Corregido: 5 de agosto de 2025 Aceptado: 29 de agosto de 2025
La cisticercosis bovina (CCB) es una enfermedad zoonótica parasitaria de importancia veterinaria y sanitaria que afecta la producción de ganado bovino en Costa Rica. El agente causal es la forma larvaria de Taenia saginata, quien necesita a los bovinos para cumplir su ciclo de vida. Este estudio tiene como objetivo determinar la distribución de casos de CCB en mataderos de exportación del país y caracterizar molecularmente T. saginata en muestras sospechosas. Se realizó un estudio transversal, analizando los reportes de retenciones y decomisos de CCB registrados por el Servicio Nacional de Salud Animal (SENASA) entre 2015 y 2019 en cuatro mataderos de exportación del país. A partir de estos datos, se identificó la cantidad y distribución de los casos en los cantones de Costa Rica. Adicionalmente, se recolectaron quistes sospechosos de CCB para realizar una detección mediante la técnica de reacción en cadena de la polimerasa (PCR). Los resultados mostraron que fueron reportados un total de 852 casos, siendo la mayoría de ellos provenientes de Alajuela (33.5%), San José (21.1%) y Guanacaste (10.8%). Los cantones de Alajuela (n=118) y San Carlos (n=90) en la provincia de Alajuela presentaron las cifras más altas de casos. Se recolectaron 24 quistes durante junio-agosto del 2020. La mayoría provenía de la provincia de Alajuela con el 58.3% hallados en músculos maseteros. El análisis por PCR detectó T. saginata en 11 muestras (45.8%), y la secuenciación reveló dos genotipos distintos, con similitudes nucleotídicas del 100% con aislamientos de Corea del Sur, Brasil, Ecuador y Bélgica, así como un genotipo que mostró similitud con un aislamiento de China. Estos hallazgos destacan la prevalencia y distribución de la cisticercosis bovina en Costa Rica, así como la importancia de implementar medidas de control y prevención efectivas.
Palabras clave: Zoonosis, mataderos de exportación, decomisos, PCR, genotipos
Bovine cysticercosis (BCC) is a parasitic zoonotic disease of veterinary and sanitary importance affecting cattle production in Costa Rica. The causal agent is the larval form of Taenia saginata, which requires cattle to complete its life cycle. This study aims to determine the distribution of BCC cases in the country’s export slaughterhouses and to characterize T. saginata in suspicious samples molecularly. A cross-sectional study was conducted, analyzing reports of CCB retentions recorded by the National Animal Health Service (SENASA) between 2015 and 2019 in four export slaughterhouses in the country. The number and distribution of cases in the cantons of Costa Rica were identified from this data. Additionally, cysts suspected of BCC were collected for detection using polymerase chain reaction (PCR). Results showed that of the 852 cases reported, the majority came from Alajuela (33.5%), San José (21.1%), and Guanacaste (10.8%). The cantons of Alajuela (n=118) and San Carlos (n=90) in the province of Alajuela had the highest number of cases. Between June and August, 24 cysts were collected, with the majority originating from the province of Alajuela, specifically 58.3% found in the masseter muscles. PCR analysis identified T. saginata in 11 samples (45.8%), and sequencing revealed two distinct genotypes. One genotype exhibited 100% nucleotide similarity with isolates from South Korea, Brazil, Ecuador, and Belgium, while the other genotype showed similarity with an isolate from China. These findings highlight the prevalence and distribution of bovine cysticercosis in Costa Rica, as well as the importance of implementing effective control and prevention measures.
Keywords: Zoonosis, export slaughterhouses, carcass condemnation, PCR, genotypes.
A cisticercose bovina (CCB) é uma zoonose parasitária de importância veterinária e sanitária que compromete a produção de gado bovino na Costa Rica. O agente etiológico é a forma larval de Taenia saginata, que necessita dos bovinos para completar seu ciclo de vida. Este estudo teve como objetivo determinar a distribuição dos casos de CCB em matadouros de exportação do país e caracterizar molecularmente T. saginata em amostras suspeitas. Realizou-se um estudo transversal, analisando os relatórios de retenções e condenações por CCB registrados pelo Serviço Nacional de Saúde Animal (SENASA) entre 2015 e 2019, em quatro matadouros de exportação do país. A partir desses dados, identificaram-se a quantidade e a distribuição dos casos nos municípios da Costa Rica. Adicionalmente, cistos suspeitos de CCB foram coletados para detecção por meio da técnica de reação em cadeia da polimerase (PCR). Os resultados mostraram que foi reportado um total de 852 casos, sendo a maioria proveniente de Alajuela (33,5%), San José (21,1%) e Guanacaste (10,8%). Os municípios de Alajuela (n=118) e San Carlos (n=90), na província de Alajuela, apresentaram os números mais altos de casos. Foram coletados 24 cistos entre junho e agosto de 2020, dos quais a maioria era procedente da província de Alajuela, com 58,3% localizados nos músculos masseteros. A análise por PCR detectou T. saginata em 11 amostras (45,8%), e o sequenciamento revelou dois genótipos distintos, com similaridade nucleotídica de 100% com isolados da Coreia do Sul, Brasil, Equador e Bélgica, além de um genótipo que mostrou similaridade com um isolado da China. Esses achados destacam a prevalência e a distribuição da cisticercose bovina na Costa Rica, bem como a importância de implementar medidas eficazes de controle e prevenção.
Palavras-chave: Zoonoses, matadouros de exportação, condenações, PCR, genótipos
Introducción
La cisticercosis bovina (CCB), ocasionada por el estadio larvario de Taenia saginata, es una enfermedad zoonótica de importancia en salud pública. La transmisión en el ganado bovino es ocasionada por los humanos que albergan al gusano adulto en su intestino y que liberan proglótidos grávidos y huevos diariamente por las heces, contaminando agua y alimentos que pueden ser ingeridos accidentalmente por los bovinos (Rossi et al., 2020).
La transmisión entre el ganado vacuno y el ser humano depende en gran medida de los hábitos de consumir carne de res cruda o insuficientemente cocida e infectada con cisticercos viables; este es un peligro potencial para la salud pública. Otros factores que favorecen y que pueden intervenir son la falta de higiene, sobre todo en países subdesarrollados, donde los animales viven y pastorean en proximidad de las viviendas humanas (Cayo-Rojas et al., 2011).
El diagnóstico de animales infectados con cisticercos de T. saginata se realiza en animales vivos mediante palpación de la lengua o post mortem en la inspección de las canales mediante examen visual e incisión o palpación de los maseteros, la lengua, el corazón, el diafragma y el esófago (obligatorio por ley en el matadero). Sin embargo, solo un pequeño número de animales es detectado por los métodos normales de incisión y palpación, ya que la sensibilidad de estos métodos es baja. Se estima que solamente un 50% de los animales y un 80-90% de los cisticercos pueden ser detectados durante la inspección de carne (Cayo-Rojas et al., 2011).
Los métodos moleculares para la confirmación de cisticercosis por T. saginata han demostrado un buen desempeño diagnóstico, aunque la sensibilidad de la técnica de reacción en cadena de la polimerasa (PCR) disminuye con la degeneración del cisticerco. Sin embargo, se ha utilizado en la identificación de las especies involucradas en el complejo teniasis-cisticercosis y también en la exclusión de otros agentes etiológicos como Echinococcus y Sarcocystis (Jardim et al., 2011). La Organización Mundial de Sanidad Animal (OMSA) recomienda el uso de PCR para la diferenciación de especies de Taenia y sugiere que esta técnica se aplique a la identificación de cisticercos (OIE, 2005).
En Latinoamérica, el problema de cisticercosis en bovinos ha sido subestimado por la falta de información pertinente, lo cual le ha restado importancia a la enfermedad. Actualmente, se desconoce la situación y la distribución de la cisticercosis en Costa Rica, por lo que este trabajo pretende determinar la distribución de la cisticercosis bovina en mataderos de exportación del país y caracterizar molecularmente T. saginata en muestras sospechosas.
Se realizó un estudio transversal, cuyo propósito fue determinar la procedencia de los casos de CCB reportados en el país durante el periodo del 2015 al 2019 y detectar molecularmente T. saginata en muestras sospechosas de mataderos de exportación de Costa Rica.
Recolecta de datos sobre cisticercosis bovina
En los cuatro mataderos de exportación del país (Montecillos, Del Valle, GICO y El Arreo) se accedió a los reportes de retenciones y decomisos de CCB realizados por el Servicio Nacional de Salud Animal (SENASA) para determinar la cantidad y distribución de los casos. Se obtuvo información sobre procedencia del animal, año de la retención o el decomiso y el matadero en el que se realizó la retención o decomiso. Los datos se digitaron en una base de datos, y con el programa Qgis, versión 3.12.1. se estableció la distribución espacial de reses positivas a T. saginata en Costa Rica.
Recolecta de quistes para análisis molecular
Entre junio y agosto del 2020 los veterinarios y el personal de inspección de cada matadero recolectaron quistes en alcohol al 70%. Los quistes fueron clasificados como viables o calcificados (Abuseir et al., 2006), se registró además la procedencia del animal y el lugar anatómico donde se encontró el quiste.
Detección molecular de T. saginata
El ADN de los quistes se extrajo utilizando el ensayo DNeasy tissue kit (Qiagen) de acuerdo con las instrucciones del fabricante, seguidamente se realizó la amplificación parcial del gen de la subunidad 1 de citocromo c oxidasa (COX1) específica para T. saginata de 827 pb siguiendo el protocolo de PCR descrito por Yamasaki et al. (2004), utilizando los cebadores: 5’-TTGATTCCTTCGATGGCTTTTCTTTTG-3’ y 5´-GACATAACATAATGAAAATG-3´. Las reacciones se llevaron a cabo en un volumen final de 50 ul, conteniendo 10 µl de ADN de la muestra, 25 µl de DreamTaq™ PCR Master Mix 2X (ThermoScientific, USA), 2 µl de cada cebador (800 nM) y 11 µl de agua libre de nucleasas. Las condiciones de PCR consistieron en una desnaturalización inicial a 95°C por 3 min seguido de 35 ciclos de 95°C por 30 s, 55°C por 30 s, 72°c por 45 s y una extensión final de 72°C por 5 min. Los amplicones se visualizaron en geles de agarosa al 1.5% teñidos con GelRed (Figueiredo et al., 2019). Los productos de PCR se enviaron a secuenciar a Macrogen, en Corea del Sur, se editaron y alinearon usando el programa Bioedit y MEGA-X, para comparar con las secuencias en la base de datos GenBank de NCBI (http://www.ncbi.nlm.nih.gov/BLAST/).
En el periodo 2015-2019 los casos de CCB reportados fluctuaron por año entre 148 a 205. para un total de 852 casos, procedentes de las siete provincias del país y registrados en los cuatro mataderos de exportación. La mayoría de los casos de CCB se encontraron en bovinos de Alajuela (33.5%), San José (21.1%) y Guanacaste (10.8%). Sin embargo, en 101 reportes (11.9%) no se indicó la procedencia del animal (Cuadro 1).
Cuadro 1. Distribución de los casos reportados de cisticercosis bovina por provincia y año en Costa Rica en el periodo 2015 al 2019
|
Provincia |
2015 n (%) |
2016 n (%) |
2017 n (%) |
2018 n (%) |
2019 n (%) |
Total n (%) |
|
Alajuela |
73 (8.6) |
61 (7.2) |
49 (5.8) |
48 (5.6) |
54 (6.3) |
285 (33.5) |
|
San José |
38 (4.5) |
35 (4.1) |
27 (3.2) |
39 (4.5) |
41 (4.8) |
180 (21.1) |
|
Guanacaste |
22 (2.6) |
22 (2.6) |
20 (2.4) |
15 (1.7) |
13 (1.5) |
92 (10.8) |
|
Puntarenas |
13 (1.5) |
10 (1.2) |
19 (2.2) |
15 (1.7) |
15 (1.8) |
72 (8.4) |
|
Limón |
11 (1.3) |
16 (1.9) |
14 (1.6) |
12 (1.4) |
19 (2.2) |
72 (8.4) |
|
Heredia |
5 (0.6) |
6 (0.7) |
8 (0.9) |
5 (0.6) |
6 (0.7) |
30 (3.5) |
|
Cartago |
7 (0.8) |
1 (0.1) |
4 (0.4) |
5 (0.6) |
3 (0.4) |
20 (2.3) |
|
S/D |
36 (4.2) |
28 (3.3) |
16 (1.9) |
9 (1.0) |
12 (1.4) |
101 (11.9) |
|
Total (%) |
205 (24.1) |
179 (21.0) |
157 (18.4) |
148 (17.4) |
163 (19.1) |
852 (100) |
*S/D: Sin datos de procedencia.
A nivel de cantón, se encontró que los cantones de Alajuela (n=118) y San Carlos (n=90) en la provincia de Alajuela presentaron la mayor cantidad de casos, seguido de los cantones de Puriscal (n=75) y Vásquez de Coronado (n=54) en la provincia de San José y Pococí en la provincia de Limón (n=50). En la Figura 1 se muestra la distribución de los casos de CCB por cantón durante el periodo del 2015 al 2019.
Cuadro 2. Quistes sospechosos de cisticercosis bovina recolectados durante junio a agosto del 2020 en mataderos de exportación de Costa Rica
|
ID |
Provincia |
Cantón |
Lugar anatómico del hallazgo |
Aspecto del quiste reportado en el matadero |
PCR |
|
01 |
Alajuela |
Zarcero |
Maseteros |
Calcificado |
Positivo |
|
02 |
Alajuela |
Upala |
Maseteros |
Calcificado |
Negativo |
|
03 |
Alajuela |
Alajuela |
Maseteros |
Viable |
Negativo |
|
04 |
Alajuela |
Alajuela |
Corazón |
Viable |
Positivo |
|
05 |
Alajuela |
Upala |
Maseteros |
Calcificado |
Negativo |
|
06 |
Alajuela |
San Carlos |
Cabeza |
Calcificado |
Negativo |
|
07 |
Alajuela |
Alajuela |
Maseteros |
Viable |
Positivo |
|
08 |
Puntarenas |
Montes de Oro |
Maseteros |
Viable |
Negativo |
|
09 |
Puntarenas |
Montes de Oro |
Corazón |
Calcificado |
Positivo |
|
10 |
Puntarenas |
Parrita |
Pterigoideo |
Calcificado |
Positivo |
|
11 |
Puntarenas |
Puntarenas |
Maseteros |
Viable |
Positivo |
|
12 |
Heredia |
Sarapiquí |
Maseteros |
Calcificado |
Negativo |
|
13 |
Heredia |
Sarapiquí |
Corazón |
Calcificado |
Positivo |
|
14 |
Heredia |
Sarapiquí |
Maseteros |
Viable |
Negativo |
|
15 |
Heredia |
Sarapiquí |
Maseteros |
Viable |
Positivo |
|
16 |
San José |
Turrubares |
Corazón |
Calcificado |
Negativo |
|
17 |
San José |
Goicoechea |
Maseteros |
Calcificado |
Negativo |
|
18 |
San José |
Vázquez de Coronado |
Maseteros |
Viable |
Positivo |
|
19 |
Guanacaste |
Cañas |
Maseteros |
Calcificado |
Negativo |
|
20 |
Guanacaste |
Liberia |
Corazón |
Calcificado |
Negativo |
|
21 |
Cartago |
Paraíso |
Maseteros |
Viable |
Negativo |
|
22 |
Cartago |
Jiménez |
SD* |
Viable |
Positivo |
|
23 |
Limón |
Pococí |
Corazón |
Calcificado |
Negativo |
|
24 |
Nicaragua |
SD* |
Corazón |
Viable |
Positivo |
*SD: sin datos.
Durante los tres meses se recolectaron un total de 24 quistes, la mayoría provenía de bovinos de Alajuela (29.2%), además se remitió un quiste de un animal importado de Nicaragua. La mayoría de los quistes (58.3%) se encontraron en los músculos maseteros y solamente 11 (45.8%) se encontraron viables. El PCR detectó la presencia de T. saginata en 11 muestras (45.8%). En el Cuadro 2 se resume la información de las muestras recolectadas durante junio a agosto del 2020.

Figura 1. Distribución de casos reportados de CCB por cantón en Costa Rica, 2015 - 2019. Los cantones con mayores casos reportados de CCB se observan con mayor intensidad de color.
La secuenciación de cinco muestras estableció la presencia de dos genotipos. Las secuencias de los quistes procedentes de Heredia (ID=13), Alajuela (ID=07) y Nicaragua (ID= 24) mostraron un 100% de identidad nucleotídica (758 pb/758 pb) con aislamientos encontrados en Corea del Sur (MK644934.1), Brasil (AB107237.1), Ecuador (AB107238.1) y Bélgica (AB107242.1), mientras que las secuencias de Cartago (ID=22) y Puntarenas (ID=10) presentaron un genotipo que presentó 100% similitud nucleotídica (758 pb/758 pb) con un aislamiento de China (AB107239.1) . En la Figura 2 se observa un dendograma del fragmento del gen COX1 de T. saginata de las cinco muestras secuenciadas.
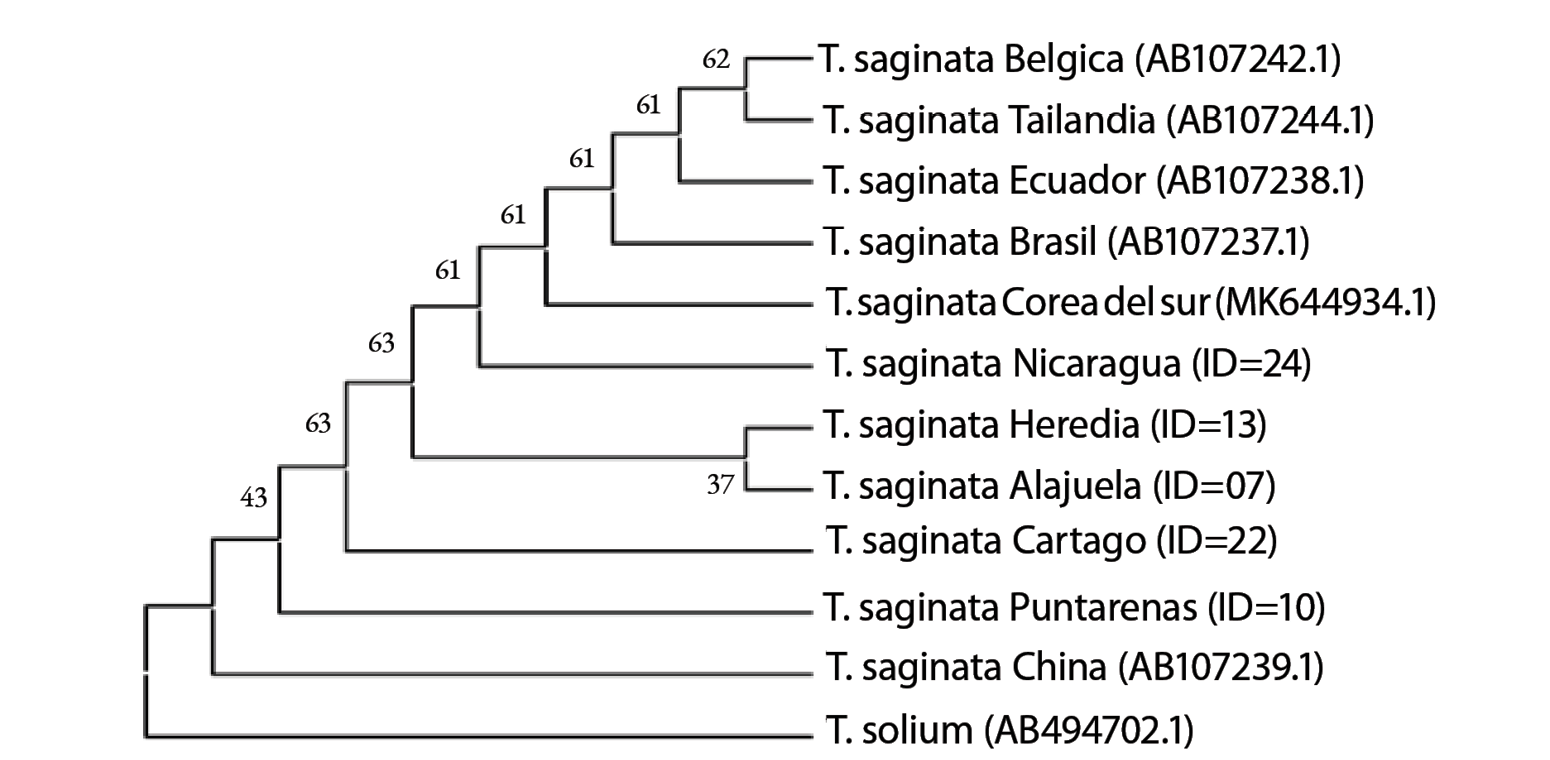
Figura 2. Dendograma de un fragmento del gen COX 1 de Taenia saginata construido por el método Neighbor joining, se incluye a T. solium como grupo externo.
Taenia saginata se encuentra distribuida en diferentes países del mundo, sobre todo los países en vías de desarrollo son los que reportan mayor presencia; esto se atribuye a un sistema pobre de higiene y saneamiento, también se atribuye a inspecciones de carne deficientes o a la ausencia de inspecciones de carne en mataderos de consumo local, como es el caso en países de América Latina (Braae et al., 2018).
Una revisión sistemática del 2018 reportó que la prevalencia de CCB se encontraba entre 0.1 y el 19 % durante el periodo de 1990 al 2017 en países de América Latina (Braae et al., 2018). En la actualidad se desconoce la distribución de este parásito o el número de casos que ocasiona el parásito en países de Centroamérica, especialmente en Costa Rica, donde no se han encontrado reportes publicados. Esto se puede atribuir, a que la enfermedad no es de notificación obligatoria a la OMSA (Organización Mundial de Sanidad Animal), en contraste con la cisticercosis porcina (Prati, 2014) y a la falta de diagnóstico parasitológico de teniasis en las heces de humanos, los cuales son los que infectan al ambiente y, por ende, los bovinos (Braae et al., 2018). La enfermedad ocasiona altas tasas de mortalidad entre el ganado bovino y causa pérdidas a la industria cárnica, debido al decomiso de las canales infectadas, ya que la carne no se considera apta para el consumo humano (Assefa & Bihon, 2019).
En la presente investigación, la CCB se encontró distribuida en las siete provincias, de acuerdo con los datos de los mataderos de exportación de Costa Rica. La información sobre la prevalencia actual de CCB en el país y en muchos países de América es desconocida; investigaciones realizadas durante el 2009 al 2010 reportan una ocurrencia de CCB de 2.019 y 148 casos en Brasil y Chile, respectivamente (Braae et al., 2018). Sin embargo, no existen datos epidemiológicos suficientes para estimar la prevalencia real y la incidencia de la enfermedad en muchos de los países de América.
Los resultados de esta investigación demuestran que Alajuela fue la provincia que presentó mayor cantidad de casos, seguido de la provincia de San José. De acuerdo con el VI Censo Nacional Agropecuario que se ejecutó en el 2014 (INEC, 2014), la provincia de Alajuela es la que posee la mayor cantidad de fincas en el país, seguida por la provincia de San José, lo que puede explicar el alto número de casos en estas provincias. Otro factor que puede estar involucrado en la transmisión de CCB es la contaminación fecal por parte de humanos con teniasis que pueda ocurrir en muchas de estas zonas, específicamente en las fuentes de agua donde puede haber una proximidad de los animales a aguas residuales, pastizales contaminados o alimentos manipulados con manos contaminadas de huevos de T. saginata. Tomando en cuenta que la CCB es transmitida principalmente de humano a bovino, resulta importante realizar encuestas epidemiológicas que determinen las prácticas higiénicas que presenta la población en estas zonas y que pueden estar involucradas en la prevalencia de la enfermedad, ya que la deficiencia o ausencia de saneamiento ambiental es clave para la contaminación ambiental por huevos y, por ende, para los bovinos.
Generalmente la teniasis en los humanos puede presentarse con síntomas leves y la CCB es generalmente asintomática, por lo que en ambos casos pasan clínicamente desapercibidos, lo cual afecta la detección temprana de ambas enfermedades (CDC, 2024). La CCB se diagnostica generalmente post mortem en los bovinos, en las inspecciones de las canales en las plantas de cosechas, lo que depende de las habilidades y conocimientos del personal (diagnóstico macroscópico). Este tipo de diagnóstico presenta limitaciones, sobre todo con quistes calcificados, ya que pueden confundirse con otros parásitos como Sarcocystis spp. y Echinococcus granulosus o por neoplasias, lo que puede ocasionar resultados falsos positivos (Cayo-Rojas et al., 2011; OIE, 2005).
El diagnóstico molecular ha demostrado ser una herramienta útil para la confirmación de CCB, sin embargo, esta técnica pierde sensibilidad con muestras de quistes calcificados. La técnica de PCR utilizada en este trabajo detectó quistes), donde la mayoría de las muestras positivas pertenecían a quistes viables, lo que concuerda con otros estudios moleculares donde reportaron una disminución de la sensibilidad con quistes calcificados por la degradación del ADN (Figueiredo et al., 2019). En la presente investigación no se pudo determinar presencia de T. saginata en 9 quistes calcificados, que probablemente eran de infecciones crónicas con escaso ADN. En cuatro casos de quistes reportados como viables tampoco se pudo demostrar la presencia de T. saginata; en estos casos no se puede descartar que las muestras tuvieran un grado de mineralización o calcificación que pudo haber interferido con el diagnóstico molecular. Sin embargo, se debe tomar en cuenta que durante la inspección post mortem se pueden presentar falsos positivos cuando se evalúan macroscópicamente los quistes, ya que existen lesiones nodulares difíciles de identificar (Figueiredo et al., 2019).
En este trabajo se compararon secuencias del gen COX1 de aislados provenientes de las provincias de Alajuela, San José, Heredia, Cartago, Puntarenas y un aislado proveniente de Nicaragua identificándose un sitio polimórfico entre ellas. Las secuencias de Alajuela, Heredia y Nicaragua pertenecían a un mismo genotipo, mientras que las secuencias de Puntarenas y Cartago pertenecían a otro genotipo, identificándose una variación en sus nucleótidos. Estudios previos, han investigado la variación genética del género Taenia mediante genes mitocondriales, entre ellos la subunidad 1 de citocromo oxidasa (COX1), siendo esta una región conservada entre el género, sin embargo, ha mostrado variabilidad a nivel de nucleótidos entre las especies de Taenia de 2.5 y el 18%. Estudios realizados por Abuseir et al. (2018) han encontrado que aislados de T. saginata de países de Asia, Sudamérica y África poseen una variación del 2.5% en el gen COX1 (Abuseir et al., 2018; Anantaphruti et al., 2013; Sanpool et al., 2017).
La migración del ganado bovino entre países cercanos puede explicar la presencia de genotipos diferentes de T. saginata en una región (Anantaphruti et al., 2013), lo cual se evidencia en este trabajo al identificarse un aislado proveniente de Nicaragua cuyo genotipo era diferente con los aislados de otras provincias de Costa Rica. Es importante llevar a cabo más estudios sobre la diversidad genética de T. saginata en el país, ya que se desconocen los genotipos presentes en las poblaciones de este parásito, no solo en Costa Rica, sino también en países cercanos. El flujo migratorio entre estas regiones podría influir en la diversidad genética observada en este estudio.
Sin embargo, este trabajo presenta algunas limitaciones. Los estudios realizados en mataderos no necesariamente reflejan la prevalencia real de la enfermedad en la población bovina de la zona, ya que el muestreo se restringe a animales destinados a sacrificio. Además, aunque se reporta la cantidad de animales infectados por año, no se dispone del número total de animales beneficiados en el mismo periodo, lo cual impide estimar con precisión la frecuencia o proporción anual de infección.
A pesar de estas limitaciones, realizar más estudios que proporcionen información sobre la CCB puede ayudar a su manejo y control, así como a conocer el impacto que tiene en la industria ganadera.
En este trabajo se reporta por primera vez la caracterización molecular de larvas de T. saginata en muestras provenientes de mataderos de exportación de Costa Rica, identificándose dos genotipos presentes en las poblaciones del parásito en el país y evidenciando como las actividades migratorias en el ganado bovino pueden afectar la diversidad genética en una población. Los resultados de este trabajo muestran la importancia del uso de técnicas moleculares como herramientas para la detección, confirmación y monitoreo de la Cisticercosis Bovina en conjunto con el diagnóstico post mortem.
Agradecimientos
A SENASA, el personal de inspección y médicos veterinarios de los mataderos Montecillos, Del Valle, El Arreo y GICO que colaboraron brindando información y recolectando las muestras. Esta investigación fue financiada con fondos del proyecto “Diagnóstico e Investigación en Medicina Poblacional y Ecosistémica” de FUNDAUNA.
Conflicto de intereses
Los autores declaramos que no poseemos conflicto de intereses con los temas expuestos.
Uso de Inteligencia Artificial
Los autores declaramos la no utilización de Inteligencia artificial en la elaboración del presente artículo.
Abuseir, S., Epe, C., Schnieder, T., Klein, G., & Kühne, M. (2006). Visual diagnosis of Taenia saginata cysticercosis during meat inspection: is it unequivocal? Parasitology Research, 99(4), 405-409. https://doi.org/10.1007/s00436-006-0158
Abuseir, S., Schicht, S., Springer, A., Nagel-Kohl, U., & Strube, C. (2018). Genetic characterization of Taenia saginata cyst isolates from Germany. Vector-Borne and Zoonotic Diseases, 18(8), 433-439. https://doi.org/10.1089/vbz.2017.2218
Anantaphruti, M., Thaenkham, U., Kusolsuk, T., Maipanich, W., Saguankiat, S., Pubampen, S., & Phuphisut, O. (2013). Genetic variation and population genetics of Taenia saginata in north and northeast Thailand in relation to Taenia asiatica. Journal of Parasitology Research, 310605. http://dx.doi.org/10.1155/2013/310605
Assefa, A. & Bihon, B. (2019). Bovine cysticercosis in Ethiopia: A systematic review and meta-analysis of prevalence from abattoir-based surveys. Preventive Veterinary Medicine. Preventive Veterinary Medicine, 169, 104707. https://doi.org/10.1016/j.prevetmed.2019.104707
Braae, U. C., Thomas, L. F., Robertson, L. J., Dermauw, V., Dorny, P., Willingham, A. L., & Devleesschauwer, B. (2018). Epidemiology of Taenia saginata taeniosis/cysticercosis: a systematic review of the distribution in the Americas. Parasites & Vectors, 11(1), 1-12. https://doi.org/10.1186/s13071-018-3079-y
Cayo-Rojas, F., Mamani-Linares, W., Gallo , C., & Valenzuela , G. (2011). A Review of Bovine Cysticercosis (Cysticercus bovis) in Cattle Slaughtered: Prevalence, Distribution and Cyst Viability. Journal of the Selva Andina Research Society, 2(1), 53-70. http://www.scielo.org.bo/pdf/jsars/v2n1/a07.pdf
CDC (Centers for Disease Control and Prevention). (2024). About Human Tapeworm (Taeniasis); Clinical Overview of Taeniasis. https://www.cdc.gov/taeniasis/about/index.html?utm_source
INEC (Instituto Nacional de Estadísticas y Censos). (2014). VI Censo Nacional Agropecuario 2014. https://inec.cr/estadisticas-fuentes/censos/censo-agropecuario-2014
Figueiredo, B. N. S., Libório, R. A., Sato, M., da SILVA, C. F., Pereira-Junior, R. A., Chigusa, Y., Kawai, S., & Sato, M. O. (2019). Occurrence of bovine cysticercosis in two regions of the state of Tocantins-Brazil and the importance of pathogen identification. Pathogens, 8(2), 66.https://doi.org/10.3390/pathogens8020066
Jardim, E. A. G. D. V., Moura, V. B. L., Vinaud, M. C., Junior, L., Junior, L., & Linhares, G. F. C. (2011). Molecular identification of Cysticercus bovis at different stages of the host-parasite interaction process. Journal of Tropical Pathology, 40(4), 331-340. https://doi.org/10.5216/rpt.v40i4.16764
OIE (World Organisation for Animal Health). (2005). WHO/FAO/OIE guidelines for the surveillance, prevention and control of taeniosis/cysticercosis. World Organisation for Animal Health. https://iris.who.int/bitstream/handle/10665/43291/9290446560_eng.pdf
Prati, B. (2014). Cisticercosis bovina en la Argentina: consideraciones respecto de su impacto económico ganadero y sanitario humano (Doctoral dissertation, Università degli Studi Di Parma y Facultad de Agronomía. UBA). http://ri.agro.uba.ar/files/download/tesis/mita/2017pratibarbara.pdf
Rossi, G. A. M., Van Damme, I., & Gabriël, S. (2020). Systematic review and meta-analysis of bovine cysticercosis in Brazil: current knowledge and way forward. Parasites & Vectors, 13(1), 1-14. https://doi.org/10.1186/s13071-020-3971-0
Sanpool, O., Rodpai, R., Intapan, P. M., Sadaow, L., Thanchomnang, T., Laymanivong, S., Maleewong, W., & Yamasaki, H. (2017). Genetic diversity of Taenia saginata (Cestoda: Cyclophyllidea) from Lao People’s Democratic Republic and northeastern Thailand based on mitochondrial DNA. Parasites & Vectors, 10(1), 1-7. https://doi.org/10.1186/s13071-017-2079-7
Yamasaki, H., Allan, J. C., Sato, M. O., Nakao, M., Sako, Y., Nakaya, K., Qiu, D., Mamuti, W., Craig, P. S., & Ito, A. (2004). DNA differential diagnosis of taeniasis and cysticercosis by multiplex PCR. Journal of Clinical Microbiology, 42(2), 548-553. https://doi.org/10.1128/JCM.42.2.548–553.2004

Licencia Creative Commons Atribución-No-Comercial